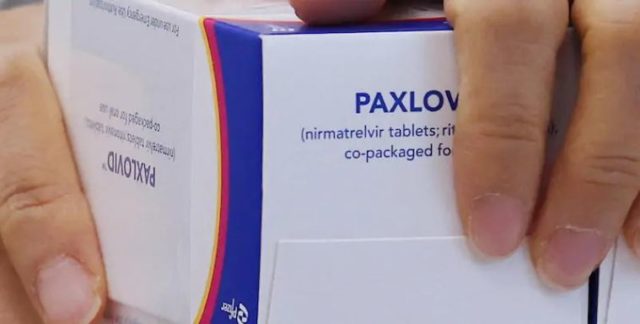
Agjencia Evropiane e Barnave (EMA) ka rekomanduar përdorimin e Paxlovid në Bashkimin Evropian. Paxlovidi është një ilaç i ri kundër Covid-19, i zhvilluar nga kompania farmaceutike amerikane Pfizer. Prandaj, në orët e ardhshme, Komisioni Evropian do të jetë në gjendje të autorizojë përdorimin e ilaçit, duke shtuar një burim të ri të rëndësishëm për të luftuar efektet e koronavirusit.
Paxlovid u autorizua në fund të dhjetorit të kaluar në Shtetet e Bashkuara, ku tani përdoret rregullisht për trajtimin e rasteve të Covid-19, megjithëse janë shfaqur disa probleme për gjetjen e tij, por prodhimi i të cilit pas miratimit të EMA-s pritet të rritet në muajt e ardhshëm.
Vaksinat janë sot mjeti më i rëndësishëm për të mbajtur nën kontroll efektet e pandemisë, deri më tani ato kanë rezultuar thelbësore për të reduktuar rastet e rënda të Covid-19, si shtrimet në spital por edhe vdekjet.
Ilaçe të tilla si Paxlovid mund të jenë ende të dobishme për njerëzit që sëmuren nga koronavirusi, por edhe për atë pjesë të qytetarëve që për shkak të problemeve të tjera shëndetësore nuk mund të vaksinohen dhe për rrjedhojë janë edhe më të ekspozuar ndaj rreziqeve të sëmundjes.
Paxlovid është një antiviral që ndërhyn në burimet e përdorura nga koronavirusi për t’u shumuar brenda qelizave tek njerëzit e infektuar.
Trajtimi konsiston në marrjen e 30 tabletave gjatë pesë ditëve të Paxlovid dhe Ritonavir, një tjetër ilaç antiviral i zhvilluar shumë kohë më parë kundër HIV. Ritonavir lejon Paxlovid të qëndrojë aktiv më gjatë në trup, duke shfaqur edhe rezultate më të mira.
Kohë më parë kompania Pfizer i kërkoi Administratës Amerikane të Ushqimit dhe Barnave (FDA) të aplikojë për përdorim urgjent ilaçin Paxlovid kundër Covid-19. Pfizer njoftoi në muajin nëntor se pilula Paxlovid e ul rrezikun e shtrimit në spital ose vdekjes nga efektet e koronavirusit me 89 për qind.
“Nëse miratimi i PAXLOVID, si ilaçi i parë antiviral oral i këtij lloji, i krijuar posaçërisht për të luftuar SARS-CoV-2, ai mund të rekomandohet për trajtimin në shtëpi të pacientëve me rrezik të lartë në shenjat e para të infeksionit“, thuhet në deklaratën e kompanisë.
Deri më sot, të gjitha trajtimet e COVID-19 të miratuara nga FDA kërkonin injeksion intravenoz nën mbikëqyrjen e profesionistëve të kujdesit shëndetësor në spitale dhe klinika.